Cellule artificiali che esprimono proteine come le loro controparti naturali
⇧ [VIDÉO] Potrebbero piacerti anche questi contenuti dei partner
I ricercatori hanno sviluppato cellule artificiali in grado di esprimere proteine come le cellule naturali. Le nuove strutture sono state sviluppate attraverso un processo chiamato autoassemblaggio indotto dalla biopolimerizzazione (bioPISA) e possono fungere da microreattori per reazioni enzimatiche e biomineralizzazione. In definitiva, queste cellule potrebbero avere importanti implicazioni in medicina e persino far luce sui misteri dell’origine della vita sulla Terra.
Nonostante i notevoli progressi compiuti negli ultimi decenni, la sintesi di cellule completamente artificiali pone molte sfide. Infatti, anche gli organismi unicellulari più semplici subiscono processi biomolecolari altamente complessi. Gli sviluppi più recenti in questo campo includono, ad esempio, parti sintetiche, che hanno consentito lo studio della trascrizione e della traduzione senza cellule. Tra queste strutture, i compartimenti polimerici biomimetici hanno particolarmente attirato l’attenzione degli scienziati, grazie alla loro maggiore stabilità rispetto ad altri assemblaggi. D’altra parte, la diversità chimica dei polimeri consente la progettazione di strutture con molteplici funzioni molecolari, come biodegradabilità, permeabilità e reattività agli stimoli.
Tuttavia, la maggior parte dei metodi di produzione di cellule artificiali basati su polimeri presenta ostacoli significativi, che ostacolano l’efficiente incapsulamento del carico funzionale. La tecnica di autoassemblaggio indotto dalla polimerasi (PISA) è stata sviluppata con l’obiettivo di superare queste limitazioni. Consiste nella produzione di copolimeri a blocchi anfifilici (che possiedono una parte idrofila e lipofila) in soluzioni acquose, polimerizzando un monomero solubile in acqua in un blocco insolubile. Più precisamente, durante la fase iniziale di polimerizzazione, il copolimero è ancora solubile in acqua. Quindi, una volta che il blocco idrofobo raggiunge una certa lunghezza, i copolimeri iniziano ad autoassemblarsi per ridurre il rapporto idrofilo/idrofobo. La morfologia delle strutture assemblate evolve in micelle e poi in vescicole, consentendo di svolgere in modo efficiente i processi di incapsulamento.
Tuttavia, nonostante la sua biocompatibilità, PISA presenta ancora dei limiti per quanto riguarda l’incorporazione di molecole biologiche nei compartimenti polimerici. Infatti, le condizioni di partenza possono compromettere l’integrità anche delle molecole più sensibili. Gli esperti delle Università di Darmstadt e Strathclyde ritengono che la tecnologia bioPISA, sviluppata nel loro nuovo studio (pubblicato su…
Chimica naturale), può contribuire a colmare queste lacune. Del gruppo di ricerca fanno parte anche ricercatori delle Università di Friburgo e Basilea, nonché dell’Istituto Adolf Merkel in Svizzera.
BioPISA consentirebbe infatti, tra le altre cose, di collegare la sintesi e l’autoassemblaggio dei polimeri attraverso PISA con processi biologici o biomimetici. ” Il nostro studio colma una lacuna cruciale nella biologia di sintesi, integrando il mondo dei materiali sintetici con processi enzimatici per creare cellule artificiali complesse, proprio come le cellule vere. », spiega in A Ho riferito L’autore principale dello studio, Andrea Beloatti, dell’Università di Strathclyde (Scozia).
“Ciò apre nuovi orizzonti nella creazione di cellule mimiche che non sono solo strutturalmente simili alle cellule biologiche ma anche funzionalmente efficienti “, Aggiunge.
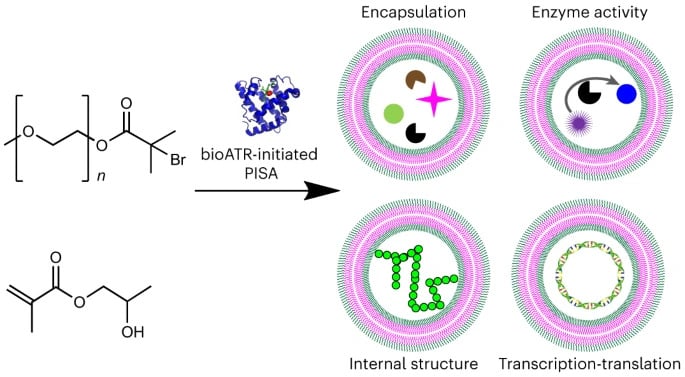
Illustrazione che mostra i passaggi per la creazione di cellule artificiali. © Andrea Beloatti et al.
Le cellule artificiali funzionano come microreattori
La tecnologia bioPISA si basa sulla polimerasi radicale a trasferimento atomico mediata da un enzima (ATRP). I catalizzatori BioATRP includono enzimi eme (un cofattore contenente un atomo di metallo) come la perossidasi di rafano, l’emoglobina, la catalasi e la laccasi contenente rame.
” La polimerizzazione enzimatica dei radicali liberi è la chiave per creare queste cellule artificiali. Gli enzimi producono polimeri che si autoassemblano durante la polimerizzazione Incapsula polimeri di dimensioni nano e micro “, spiega il coautore dello studio Nicholas Bruns, dell’Università di Strathclyde e Darmstadt. Questo è un metodo molto semplice ma efficace per preparare cellule artificiali “, Annunciare.
Per assemblare cellule artificiali, il nuovo metodo utilizza la mioglobina per indurre la sintesi di copolimeri a blocchi anfifilici, che si autoassemblano in micelle e vescicole unilamellari giganti (GUV). La mioglobina è stata scelta come biocatalizzatore perché è una proteina piccola e stabile che può funzionare a pH relativamente neutro. Al contrario, l’emoglobina necessita di un pH acido per acquisire proprietà simili, che non sono necessariamente biologicamente rilevanti.
Guarda anche

Durante la polimerizzazione, le GUV risultanti sono state in grado di incapsulare con successo carichi di contenuti solubili (cioè citosol) di cellule batteriche, inclusi enzimi, nanoparticelle, microparticelle, plasmidi e lisati cellulari. Le cellule artificiali risultanti servivano da microreattori per reazioni enzimatiche e biomineralizzazione (ad esempio cellule ossee).
Inoltre, erano in grado di esprimere proteine fluorescenti e actina quando nutriti con aminoacidi. Inoltre, attraverso la polimerizzazione intracellulare, l’actina ha modificato la loro struttura creando sottocompartimenti interni, formando impalcature simili al citoscheletro. Ciò suggerisce che queste cellule potrebbero imitare i batteri naturali, perché sono costituite da un compartimento di reazione microscopico, che contiene informazioni per l’espressione proteica.
Questi risultati non solo indicano che l’espressione delle proteine imita quelle che governano le proprietà fondamentali delle cellule viventi, ma evidenziano anche il potenziale di queste cellule artificiali in diverse applicazioni, dalla somministrazione di farmaci all’ingegneria dei tessuti, senza contare la comprensione della manifestazione della vita. Successivamente, i ricercatori intendono esplorare l’espressione di queste proteine per stimolare un’ulteriore polimerizzazione, con l’obiettivo di imitare la crescita e la replicazione delle cellule normali.
fonte : Chimica naturale

“Pioniere del caffè a misura di hipster. Creatore amichevole. Analista pluripremiato. Scrittore. Studioso di cibo. Drogato di televisione. Ninja di Internet.”
